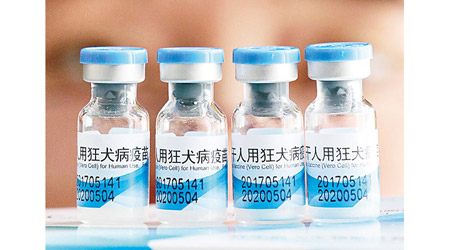
行動升級人大修例杜絕長生翻版 製售假疫苗重罰3560萬
吉林長春長生生物科技公司去年被揭發疫苗造假,引起全社會關注問題疫苗。第十三屆全國人大常委會第十次會議昨日(20日)起一連三日在北京舉行,其中對《疫苗管理法》修改草案進行第二次審議,二審草案較一審作出修改,包括升級對生產及銷售假劣疫苗等違法行為的處罰,提高罰款金額,最高可罰三千萬元(人民幣.下同,約三千五百六十萬港元),以增加違法成本。
草案指,疫苗不同於一般藥品,直接關係到公共安全,應加大對違法行為的懲罰力度,而生產、銷售假劣疫苗、提供虛假資料及違反藥品質量監管等違法行為,應提高罰款額度。
草案規定,如生產、銷售的疫苗屬於假疫苗,罰款標準為違規疫苗貨值金額十五倍以上、三十倍以下的罰款;貨值金額五十萬元(約五十九萬港元)以上、不足一百萬元(約一百一十九萬港元)的,處以五百萬元(約五百九十四萬港元)以上、三千萬元以下的罰款。
追溯接種資料至少5年
針對疫苗過期、掉包事件,草案亦加強監管,明確要求將「三查七對」和追溯接種資料等寫入法律草案。「三查七對」是指醫護人員為民眾接種疫苗前,要按照接種工作規範的要求,檢查接種人士的健康狀況和接種禁忌,查對針卡,檢查疫苗、注射器外觀、批號、有效期,核對接種者的姓名、年齡,以及疫苗名稱、規格、劑量、打針部位及途徑等。同時要確保接種資料可追溯,紀錄保存時間不得少於五年。
打針反應異常可獲賠償
草案還完善懲罰性賠償規定,若明知疫苗有質量問題仍然銷售、接種,造成接種者死亡或者健康嚴重損害的話,接種者或者其親屬除要求賠償損失外,還可以要求相應的懲罰性賠償。新增國家實行預防接種異常反應補償制度規定,接種過程中或之後出現接種者死亡、嚴重殘疾、器官組織損傷等損害,若屬於接種異常反應,應當給予補償。
本報綜合報道